Le soluzioni rigenerative Straumann® sono il nostro contributo per la rigenerazione dei tessuti duri e molli intorno ai denti o agli impianti dentali e per mantenere una funzione e un'estetica durature. Non siamo un fornitore qualsiasi; siamo qui per sostenerti fornendo soluzioni scientificamente fondate per casi semplici e complessi di preservazione dei denti, gestione del sito implantare e preservazione degli impianti.
Aree principali
Panoramica del portfolio
Altre informazioni
Casi clinici e articoli scientifici che trattano le soluzioni rigenerative Straumann® nella nostra rivista online.


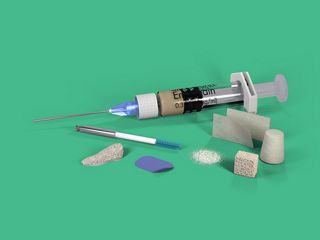
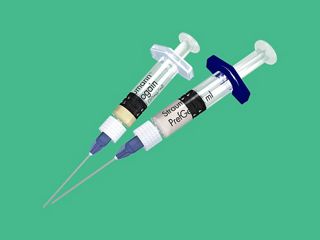
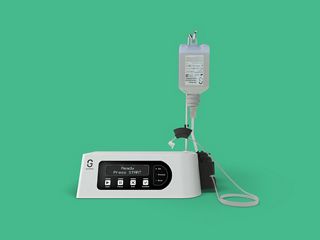
Portfolio Straumann® di prodotti per soluzioni rigenerative
Scopri il portfolio delle soluzioni rigenerative Straumann®.